Jenis sel volta sangat bermanfaat. Di kehidupan sehari-hari, jenis dari sel volta ini sering digunakan. Dalam kimia, kebutuhan akan sel ini juga cukup vital. Anda pasti sudah tahu apa itu energi listrik. Bahkan energi listrik ini menjadi salah satu kebutuhan sehari-hari.
Sumber kebutuhan listrik itu berasal dari pembangkit listrik. Namun, ada juga berbagai sumber listrik yang sangat bermanfaat lainnya.
Seperti misalnya dari reaksi kimia atau yang terkenal sebagai elektrokimia. Reaksi elektrokimia ini berlangsung pada sebuah sel yang bernama sel elektrokimia.
Baca Juga: Elektrokimia dan Aplikasinya yang Bermanfaat di Kehidupan
Sel elektrokimia tersebut ada dua, yaitu sel volta dan sel elektrolisis. Kini kita akan membahas lebih lanjut mengenal sel volta.
Jenis Sel Volta Apa Saja?
Kimia adalah salah satu sumber ilmu yang sangat bermanfaat di kehidupan. Salah satu manfaat dari reaksi kimia adalah menimbulkan energi listrik.
Bagian dari elektrokimia tersebut adalah sel volta. Sel volta adalah sel yang mampu menghasilkan energi listrik.
Untuk menghasilkan energi listrik, sel volta ini membutuhkan keberadaan redoks spontan. Dengan kata lain, sel volta akan sangat mempengaruhi energi kimia menjadi energi listrik.
Cara Kerja Sel Volta
Sebelum membahas lebih lanjut, mari melihat bagaimana sel kimia ini bekerja. Sel volta sebenarnya bekerja karena adanya prinsip dua logam.
Ketika ada dua logam yang berbeda di dalam satu larutan elektrolit, maka logam akan bersifat reaktif hingga memiliki tendensi.
Nah, tendensi tersebut akan terlarut di dalam larutan elektrolit sebagai ion logam yang positif dan dapat meninggalkan elektron pada plat logam.
Alhasil, logam akan bersifat reaktif dan muatan negatif. Sementara logam akan bersifat non reaktif dan juga mampu menarik ion positif dalam larutan elektrolit.
Berikut ini beberapa jenis sel volta yang dibutuhkan dalam kehidupan sehari-hari.
Jenis Sel Sekunder
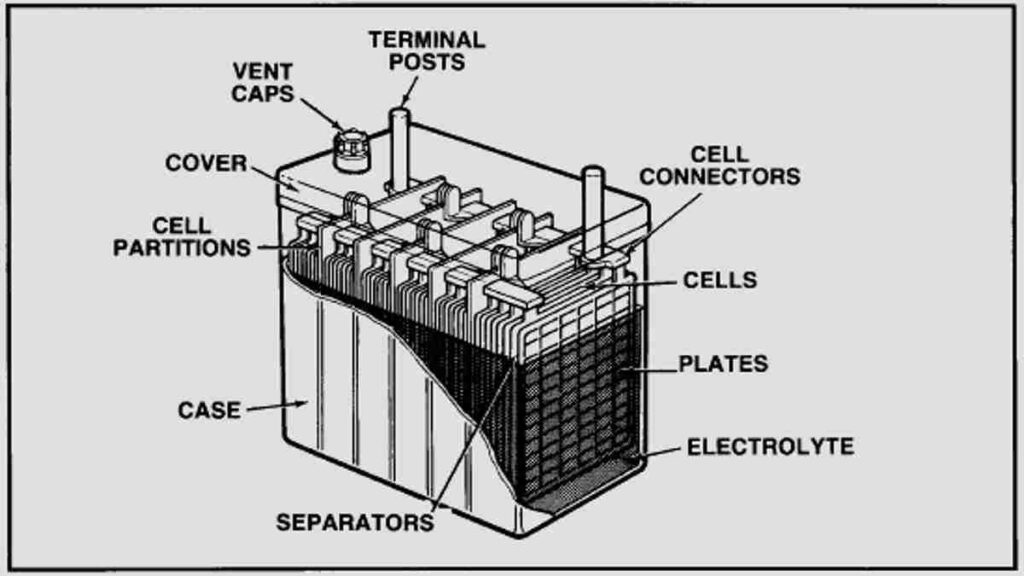
Pertama ada sel sekunder. Ini adalah sel yang dapat terisi kembali (isi ulang) secara elektrik apabila sudah digunakan untuk kembali ke kondisi semula.
Baca Juga: Perbedaan Sel Volta dan Sel Elektrolisis, Simak di Sini!
Proses isi ulang tersebut dengan mengalirkan arus melalui rangkaian yang memiliki arah berlawanan dengan arus selama pelepasan.
Reaksi redoks akan berlangsung pada sel sekunder dan bersifat reversibel atau dapat terbalik.
Contoh dari sel sekunder ini cukup bermanfaat di kehidupan yaitu accumulator atau yang terkenal sebagai aki, baterai ion litium, dan juga Ni- Cd.
Sel Bahan Bakar
Jenis sel volta yang selanjutnya adalah sel bahan bakar. Sel ini mirip seperti baterai, kecuali semua bahan aktif yang masuk ke dalam baterai berasal dari sumber luar.
Keberadaan sel bahan bakar ini berbeda dari baterai karena memang memiliki kemampuan untuk menghasilkan energi listrik yang memiliki bahan aktif masuk di dalam elektrode.
Baterai akan berhenti beroperasi apabila tidak ada bahan aktif yang masuk. Pengaplikasian sel bahan bakar yang paling terkenal adalah bahan bakar kriogenik.
Bahan bakar kriogenik tersebut sangat berguna dalam kendaraan luar angkasa. Tidak heran jika sel bahan bakar ini termasuk sangat bermanfaat.
Sel Primer

Jenis sel volta berikutnya adalah sel primer atau baterai. Ini adalah sel yang tidak dapat dengan mudah terisi ulang.
Apabila sudah menggunakan sel primer, maka paling efektif adalah membuangnya. Sebagian besar sel primer akan menggunakan elektrolit yang terkandung di dalam bahan penyerapan atau pemisah.
Karena tidak ada elektrolit yang cair, maka sel primer juga terkenal sebagai sel kering.
Baca Juga: Contoh Sel Elektrolisis serta Bagian-bagiannya, Ini Dia Penjelasannya!
Adapun reaksi redoks pada sel primer ini memiliki sifat tidak dapat terbalik atau irresistible. Contoh dari sel primer adalah sel yang kering, seperti baterai perak oksida, baterai merkuri oksida, dan baterai biasa.
Dapat terlihat bahwa sel volta ini sangat bermanfaat di kehidupan. Sel volta dapat menimbulkan arus listrik dari proses kimia yang terjadi.
Secara sederhana, sel volta ini terjadi karena keberadaan transfer elektron yang ada di reaksi redoks secara langsung. Sel volta dapat memiliki reaksi oksidasi dan juga redoks yang spontan
Keberadaan jenis sel volta tersebut sangat bermanfaat di kehidupan sehari-hari, bahkan pemanfaatannya pun sudah banyak kita temukan. Reaksi kimia yang terjadi akan menimbulkan arus listrik selain dari pembangkit listrik lainnya. (R10/HR-Online)







