Titrasi asam basa mungkin sudah cukup familiar. Istilah titrasi larutan asam basa ini sering muncul ketika mempelajari kimia. Metode kimia ini sangat penting dalam menentukan sifat atau moralitas dari sebuah larutan.
Perlu Anda ketahui bahwa titrasi merupakan sebuah metode laboratorium umum yang berguna untuk menganalisis kimia kuantitatif. Hal ini merupakan metode yang sering dilakukan.
Pada dasarnya metode titrasi berfungsi untuk menentukan apa konsentrasi titran. Dengan melakukan titrasi, maka nantinya kita dapat mengetahui apakah larutan tersebut termasuk jenis kedua larutan ini.
Baca Juga: Kesetimbangan Asam Basa dalam Kimia Dasar, Ini Dia Penjelasannya!
Memahami Proses Titrasi Asam Basa
Dalam kimia, titrasi merupakan suatu prosedur yang dapat menentukan kadar suatu larutan. Di dalam titrasi, larutan yang volumenya teratur bisa kita reaksikan secara bertahap dengan larutan lainnya yang kadarnya sudah jelas (larutan standar).
Berdasarkan jenis reaksi yang akan terjadi, titrasi terbagi menjadi asam basa, pengendapan, dan titrasi redoks. Kali ini kita akan membahas jenis asam basa.
Titrasi jenis ini merupakan sebuah metode analisa kimia yang secara kuantitatif seringkali berguna di dalam laboratorium.
Fungsi dari titrasi ini adalah untuk menentukan reaktan dan juga konsentrasi. Titrasi merupakan larutan yang netral di dalam proses titrasi. Selain itu, ada juga titran yang sebagai larutan untuk ditentukan titrasinya.
Peralatan untuk melakukan titrasi bernama titrasi meter. Kemolaran akan menyatakan bahwa jumlah mol zat larut dari setiap liter larutan serta bisa untuk menentukan pengenceran sebuah larutan.
Di dalam ilmu kimia, larutan asam basa ini sering berfungsi untuk menentukan seberapa besar nilai pH dari sebuah larutan.
Pada satu reaksi titrasi asam basa yang telah selesai, maka jumlah zat suatu reaktan akan sama dengan yang bereaksi pada jumlah zat reaktan lainnya. Berikut rumusnya:
Mol asam = Mol basa dengan Mol yang dapat Anda peroleh dengan Mol = konsentrasi x volume.
Dari persamaan tersebut, Anda bisa memasukkannya ke dalam rumus pertama:
Mol asam (konsentrasi x volume asam) = Mol basa (konsentrasi x volume basa).
Selain itu, Anda juga bisa menggunakan rumus Ma x Va x na = Mb x Vb x nb
Baca Juga: Teori Asam Basa Lewis dalam Kimia, Apa Kelebihan yang Dimilikinya?
Apa Hasil Titrasi Asam Basa?
Pada titrasi jenis ini, apabila larutan asam kuat mendapatkan titrasi dengan basa kuat, maka akan menghasilkan pH yang netral.
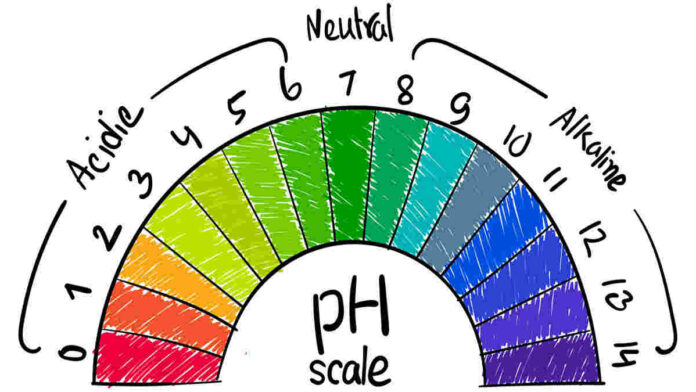
Namun, apabila larutan asam kuat mendapatkan titrasi oleh basa lemah, hasilnya akan bersifat asam atau pH kurang dari 7. Berikut daftar pH yang akan Anda dapatkan dengan kertas lakmus:
- Tingkat pH 1-3 = asam kuat dengan warna merah
- pH 4-5 = asam lemah dengan warna orange.
- Tingkat pH 6 = asam sangat lemah dengan warna kuning
- pH 7 = netral dengan warna hijau
- Tingkat pH 8 = basa sangat lemah dengan warna biru
- pH 9-10 = basa lemah dengan warna ungu
- Tingkat pH 11-14 = basa kuat dengan warna violet.
Titrasi Alkalimetri
Alkalimetri merupakan jenis titrasi asam basa dengan menggunakan larutan standar berupa basa. Titrasi ini paling umum digunakan oleh banyak orang.
Pada reaksi ini, larutan standarnya adalah basa kuat dengan zat terlarut atau sampelnya adalah asam lemah. Dengan begitu, hasil pH akan lebih dari 7 adalah pH basa.
Contoh titrasi alkalimetri yang paling umum adalah reaksi antara HCl dengan NaOH.
Baca Juga: Indikator Alami Asam Basa, Menggunakan Ekstrak Tumbuh-Tumbuhan
Titrasi Asidimetri
Tidak hanya alkalimetri, jenis titrasi larutan asam basa lainnya adalah asidimetri. Jenis titrasi ini merupakan kebalikan dari sebelumnya.
Titrasi asidimetri merupakan jenis titrasi dengan menggunakan larutan standar berupa asam. Pada titrasi jenis ini, larutan asam kuat akan kita titrasikan dengan basa kuat.
Dengan demikian, hasil pH dari titrasi asidimetri adalah netral. Akan tetapi, jika larutan asam kuat mendapatkan titrasi basa lemah, maka hasil dari pH akan kurang dari 7 atau bersifat asam.
Contoh titrasi asidimetri satu ini dapat terjadi di larutan amonium hidroksida atau NH4OH yang termasuk basa lemah. Larutan tersebut kemudian melalui proses titrasi dengan larutan asam klorida (HCl) yang termasuk asam kuat.
Memahami titrasi asam basa ini sangat penting untuk Anda yang memang tertarik dalam bidang kimia. Umumnya praktek titrasi ini bahkan sudah masuk ke dalam kurikulum pendidikan sekolah menengah. (R10/HR-Online)