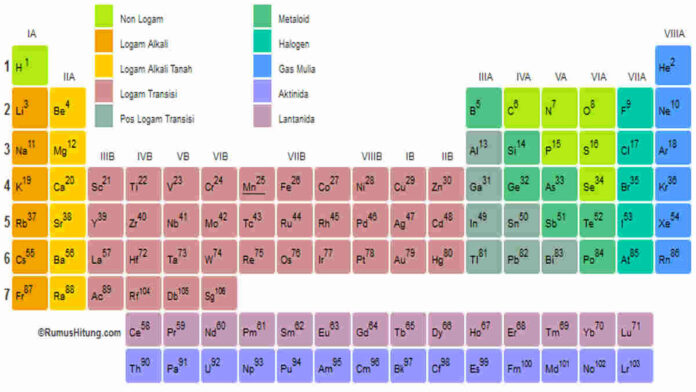
Sifat periodik unsur sangat luar biasa. Periodik unsur memiliki sifat yang berkaitan dengan letak atau posisi suatu unsur tersebut. Di dalam tabel periodik, suatu unsur memiliki posisi yang sesuai dengan sifat-sifatnya.
Anda pasti sudah pernah melihat tabel periodik. Di buku pelajaran atau lab sekolah seringkali muncul tabel periodik yang berisi berbagai macam unsur di dalamnya.
Bahkan beberapa juga ada yang pernah mencoba menghafalnya. Meski sudah cukup familiar, apakah Anda tahu bahwa unsur yang ada di dalam tabel periodik tersusun sesuai dengan sifatnya? Berikut penjelasannya!
Baca Juga: Sifat Kimia Alkena, Jenis Reaksi, Berserta Sifat Fisikanya!
Bagaimana Sifat Periodik Unsur?
Setiap unsur memiliki sifat mereka sendiri. Sifat tersebut bahkan berkaitan dengan letak atau posisi mereka pada tabel periodik.
Jenis sifat pada unsur meliputi sifat-sifat atom yang berhubungan secara langsung dengan struktur atom tersebut.
Apabila mengutip dari Wikipedia, sistem periodik dari unsur juga terkenal sebagai periodisitas sifat unsur memiliki arti sebagai pengelompokan dari unsur-unsur berdasarkan kemiripan karakternya.
Kemiripan tersebut mencakup sifat dari atom maupun senyawanya. Kemudian, perolehan unsur tersebut juga berasal dari berbagai wujud serta bentuk atom dan ion.
Semua sifat-sifat yang ada di dalam tabel periodik memiliki keteraturan. Berikut ini sifat-sifatnya:
Jari-Jari Atom
Sifat yang pertama adalah jari-jari atom, yaitu jarak dari inti atom dengan bagian terluar dari elektron. Jarak tersebut dapat diukur dalam satuan pikometer dan angstrom.
Di dalam satu golongan dari atas kebawah, jari-jari atom akan cenderung membesar setara dengan pertambahan daripada kulit elektron.
Meski muatan intinya bertambah positif, tetapi tetap jumlah kulit semakin banyak dari atas ke bawah. Kondisi tersebut membuat gaya tarik oleh inti pada elektron terluar semakin melemah.
Selain itu, sifat periodik unsur jari-jari atom juga cenderung lebih kecil dari kiri ke kanan. Padahal, jumlah elektron justru bertambah dari kiri ke kanan juga.
Dengan bertambahnya muatan inti dan masih menempati kulit yang ada, gaya tarik inti elektron akan semakin kuat. Alhasil jari-jari atom semakin mengecil.
Baca Juga: Ciri Khas Atom Karbon yang Istimewa, Apa Saja Itu?
Afinitas Elektron
Muatan inti akan bertambah positif, sehingga jari-jari atom membesar. Kemudian, daya menarik elektron oleh inti juga semakin melemah dan menyebabkan elektron berkurang.
Afinitas elektron memiliki arti sebagai energi yang terhubung ketika suatu unsur menerima elektron dalam kondisi gas. Sifat periodik unsur satu ini cenderung berkurang dari atas ke bawah pada satu golongan.
Dalam satu periode afinitas, arah kanan akan cenderung bertambah. Muatan inti akan berubah menjadi tambah positif.
Sementara itu, jumlah kulit yang tetap membuat gaya tarik dari inti terhadap elektron yang tertangkap semakin kuat. Akhirnya terjadinya afinitas elektron yang semakin bertambah.
Energi Ionisasi
Ini merupakan jenis energi yang diserap dan bertujuan untuk melepas satu elektron dari sebuah atom. Di sisi lain, energi ionisasi atom kedua merupakan energi yang diserap untuk melepas elektron kedua dari sebuah atom, dan seterusnya.
Sifat periodik unsur ini merupakan energi minimal yang penting dalam proses pelepasan elektron paling luar dari atom dengan wujud gas di kondisi dasarnya.
Terdapat kecenderungan dalam suatu golongan energi ionisasi, yaitu semakin kecil dari atas ke bawah. Hal itu karena jari-jari atom yang bertambah besar.
Meski jumlah positif bertambah, tetapi gaya menarik elektron terluar oleh inti semakin lemah karena jari-jari yang semakin panjang. Akibatnya adalah energi ionisasi akan berkurang.
Selanjutnya, dalam periode untuk energi ionisasi unsur akan cenderung membesar dari kiri ke kanan karena muatan positifnya bertambahnya pada inti dan jumlah kulitnya tetap.
Baca Juga: Senyawa Kovalen Polar: Pengertian, Sifat, Ciri Beserta Contohnya
Keelektronegatifan
Sifat selanjutnya ini merupakan kemampuan atau kecenderungan dari sebuah atom dalam menarik elektron di dalam suatu ikatan kimia.
Nilai keelektronegatifan yang semakin besar artinya ikatan kimia tersebut memiliki kecenderungan menarik elektron dari atom lainnya.
Keelektronegatifan suatu unsur di dalam satu golongan juga akan semakin berkurang dari atas ke bawah. Jumlah muatan inti akan menjadi positif dan jumlah kulit ikut bertambah.
Selanjutnya, untuk kecenderungan keelektronegatifan unsur atom juga mengalami kenaikan dari kiri ke kanan Muatan dari inti semakin positif dan jumlah kulit tetap yang menyebabkan gaya menarik elektron semakin kuat oleh inti.
Dengan demikian, sifat periodik unsur ini akan membuat atom mengalami kemampuan dalam menarik elektron yang semakin besar. (R10/HR-Online)