Senyawa yang memiliki ikatan kovalen sangat beragam. Senyawa dengan ikatan kovalen ini memiliki ciri tersendiri. Adapun ikatan kovalen ada di dalam materi kimia.
Ikatan kovalen dapat terbentuk di antara dua jenis atom yang memiliki elektronegativitas sama ataupun keduanya yang memiliki elektronegativitas kecil.
Baca Juga: Contoh Senyawa Alkuna Beserta Manfaatnya di Kehidupan!
Istilah satu ini mungkin sudah tidak asing untuk sebagian orang. Sebab, ikatan kovalen berkaitan erat dengan materi kimia maupun fisika.
Senyawa yang Memiliki ikatan Kovalen di Dalam Kimia
Di dalam kimia terdapat berbagai jenis senyawa yang terbentuk karena keberadaan satu atau bahkan lebih unsur yang saling berikatan.
Salah satu ikatan yang ada di dalam kimia adalah ikatan kovalen. Ikatan kovalen ini menjadi salah satu materi yang sangat penting di dalam kimia.
Pada tahun 1900-an, para profesor kimia dan fisika melakukan penelitian. Mereka meneliti bagaimana atom dapat bergabung dan membentuk senyawa atau molekul.
Kesimpulan dari penelitian tersebut adalah atom yang membentuk suatu ikatan kimia. Ikatan kimia tersebut memiliki gaya tarik-menarik agar atom tetap bersama.
Apa Itu Ikatan Kovalen?
Sebelum mengetahui jenis-jenis senyawa yang termasuk senyawa kovalen, tentu saja Anda perlu memahami apa sebenarnya yang dimaksud dari senyawa kovalen itu sendiri.
Ikatan kovalen adalah suatu ikatan yang terbentuk atas dua atom dengan selisih elektronegativitas kecil. Lalu terjadinya ikatan kovalen pada senyawa adalah akibat dari penggunaan bersama pasangan elektron.
Dua atom menggunakan pasangan elektron dan berkaitan untuk mencapai konfigurasi elektron stabil. Ikatan kovalen ini terjadi antara atom non logam atau semi logam dan juga non logam.
Berikut ini contoh senyawa yang memiliki ikatan kovalen di dalamnya!
Contoh Senyawa dengan Ikatan Kovalen Tunggal
Sebenarnya ada banyak senyawa yang terbentuk dengan ikatan kovalen. Adapun terdapat ikatan kovalen tunggal maupun ikatan kovalen koordinasi.
Dalam ikatan kovalen tunggal, semua unsur golongan halogen akan membentuknya pada molekul diatomik. Artinya semua molekul diatomik halogen memiliki ikatan kovalen tunggal.
Baca Juga: Senyawa Organik dan Anorganik: Definisi dan Perbedaannya!
Senyawa diatomik halogen tersebut meliputi:
- Senyawa fluorin (F2)
- Klorin (CI2)
- Senyawa Bromin (Br2)
- lodin (l2)
Selain itu, senyawa ikatan kovalen tunggal juga terdapat di senyawa selain diatomik halogen. Contoh ikatan kovalen tersebut adalah gas hidrogen (H2).
Di dalam senyawa yang memiliki ikatan kovalen ini, setiap atom H membentuk H2 akan memiliki satu elektron valensi. Kemudian atom H juga membutuhkan dua elektron untuk mengisi kulit valensi setiap atom secara penuh.
Contoh Senyawa Ikatan Kovalen Koordinasi
Selanjutnya adalah contoh senyawa dengan ikatan kovalen koordinasi. Ikatan kovalen satu ini adalah ikatan kimia yang dapat terjadi akibat dari pasangan elektron bersama yang kedua atom gunakan berasal dari salah satu atom saja.
Dengan demikian, atom lainnya akan berfungsi sebagai penerima elektron yang berpasangan di dalam ikatan kovalen koordinasi.
Berikut ini beberapa contoh senyawa yang memiliki ikatan kovalen lainnya:
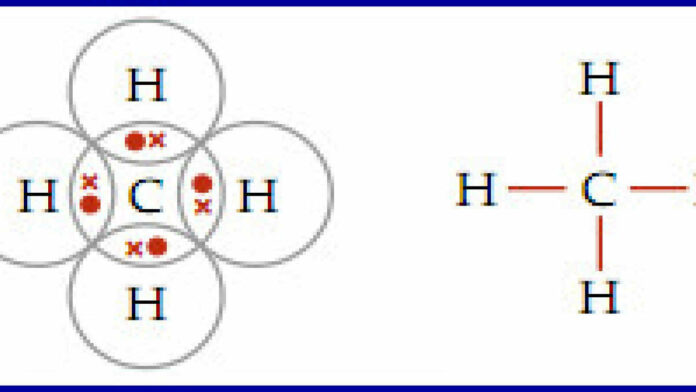
- Senyawa Metana (CH4)
- Oksigen (CO2)
- Senyawa Air (H2O)
- Amonia (NH3)
- Senyawa Etana (C2H6).
- Asam Klorida (HCl)
- Senyawa Asam Fluorida (HF)
Perbedaan Senyawa Ionik dan Senyawa Kovalen
Selain ikatan kovalen, ada juga ikatan ionik dengan jeni senyawa yang berbeda juga. Keduanya tentu memiliki perbedaan sifat fisika maupun kimia.
Perbedaan yang paling identik adalah titik leleh dan didihnya. Senyawa ionik memiliki titik leleh dan titik didih tinggi, sedangkan senyawa kovalen endah.
Dalam keadaan kamar, senyawa kovalen berbentuk padat, cair, maupun gas. Sedangkan senyawa ionik akan berwujud padat.
Perbedaaan lainnya adalah pada kelarutannya. Pada pelarut polar, senyawa kovalen tidak akan bisa larut, sedangkan senyawa ionik dapat larut. Adapun contoh dari pelarut polar adalah air.
Meski demikian, tentu saja senyawa kovalen ini masih bisa tetap larut dengan pelarut non-polar. Adapun senyawa kovalen tidak bisa menghantarkan daya hantar listrik lelehan, tetapi bisa menghantarkan daya hantar listrik larutan.
Keelektronegatifan menjadi salah satu kecenderungan suatu atom untuk bermuatan negatif atau kemampuannya untuk melisih elektronegativitas kecenangkap elektron dari jenis atom lainnya.
Baca Juga: Sifat Kimia Alkena, Jenis Reaksi, Berserta Sifat Fisikanya!
Nilai dari keelektronegatifan suatu benda dapat terlihat dari skala pauling. Skala tersebut dapat membantu melihat tinggal keelektronegatifan suatu atom atau senyawa.
Tentu saja ada berbagai contoh senyawa yang memiliki ikatan kovalen. Selalu ingat bahwa senyawa tersebut juga memiliki fungsi tersendiri di kehidupan. (R10/HR-Online)