Contoh ikatan hidrogen merupakan salah satu materi kimia yang umum. Selain ikatan hidrogen, ada juga ikatan ion dan ikatan kovalen.
Kedua ikatan tersebut berdasarkan pada konfigurasi elektron yang berasal dari atom-atom penyusunnya. Atom-atom tersebut bergabung melalui ikatan ion maupun kovalen dalam membentuk molekul.
Pada tingkat molekul tersebutlah ikatan lain dapat terbentuk dari interaksi atom hidrogen dengan atom yang memiliki pasangan elektron bebas.
Atom bebas tersebut bisa berada dalam satu molekul maupun molekul lain. Ikatan tersebutlah yang bernama ikatan hidrogen. Apa itu sebenarnya?
Baca Juga: Hukum Kekekalan Massa Kimia: Sejarah, Bunyi, Beserta Contohnya
Contoh Ikatan Hidrogen dan Pengertiannya
Kimia memiliki banyak hal untuk kita pelajari, salah satunya adalah bab ikatan. Pada bab ikatan inilah terdapat ikatan hidrogen.
Ikatan hidrogen merupakan ikatan yang terjadi di antara atom H dengan atom lain. Atom lain tersebut harus memiliki pasangan elektron bebas atau keelektronegatifan tinggi seperti halnya Cl, N, F, dan O.
Terjadinya ikatan hidrogen bisa di satu molekul maupun antar molekul.
Ikatan hidrogen yang ada dalam suatu molekul umumnya sering terjadi pada senyawa organik.
Senyawa tersebut antara lain yang mengandung dua gugus -H dengan jarak tidak terlalu jauh, misalnya saja asam oksalat (H2C2O4).
Kemudian adanya ikatan hidrogen ini kemudian akan membuat titik didih senyawa akan lebih tinggi. Kekuatan ikatan hidrogen memang akan lebih lemah daripada ikatan ion maupun kovalen.
Namun, ikatan hidrogen akan lebih kuat daripada gaya van der Waals.
Untuk lebih jelasnya, berikut ini beberapa contoh ikatan hidrogen.
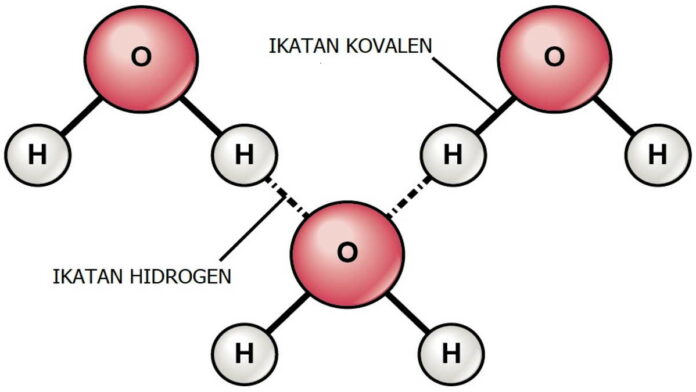
- H2O, ikatan hidrogen pada senyawa ini terjadi melalui atom H dengan atom O molekul lain.
- HF, ikatan hidrogen pada senyawa ini terjadi melalui atom H dengan atom F dari molekul lain.
- CH3COOH, ikatan hidrogen satu ini terjadi melalui atom O dari C=O dengan atom H yang berasal dari gugus -OH molekul lain.
Baca Juga: Pengertian Isotop dan Contohnya di Kimia, Ketahui Keseimbangannya!
Ikatan Hidrogen dan Sifat Fisis
Sifat fisis seperti halnya titik didih dan titik lebur sangat bisa terpengaruh oleh gaya interaksi antar-molekul.
Dengan keberadaan ikatan hidrogen maka sebagai gaya yang paling kuat interaksi antar-molekul, maka akan memberi pengaruh yang cukup signifikan terhadap titik didih. Kemudian juga terhadap beberapa senyawa hidrida biner, serta berbagai unsur golongan IVA hingga VIIA.
Titik didih dari senyawa hidrida dalam golongan IVA seperti GeH4 dan SnH4, serta nonpolar akan meningkat dari atas ke bawah golongan (dari C ke Sn).
Itu bisa saja terjadi karena adanya polarisabilitas dan juga gaya dispersi London. Gaya tersebut kemudian meningkat seiring bertambahnya massa molekul.
Baca Juga: Pengertian Zat Tunggal Dalam Kimia yang Terdiri dari Unsur dan Senyawa
Senyawa-senyawa hidrida golongan VIA, VA, dan juga VIIA mengikuti pola yang sama pada kenaikan titik didih. Akan tetapi khusus senyawa H2O, NH3, dan HF memiliki titik didih yang lebih tinggi dari yang lainnya.
Nah, itulah pengertian, contoh ikatan hidrogen, bahkan hingga ke sifat fisisnya yang bisa kamu pelajari kapan saja. (R10/HR-Online)