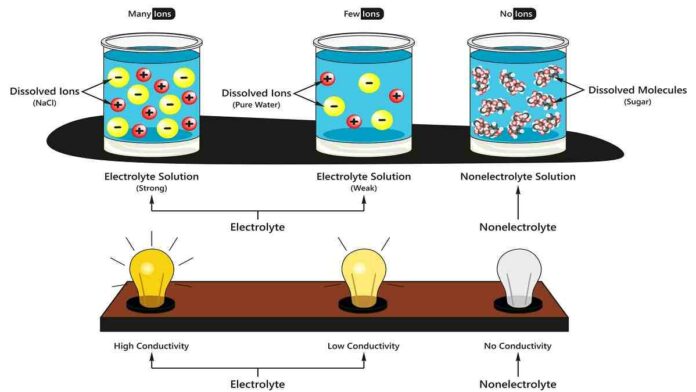
Ada berbagai jenis larutan elektrolit yang dapat menghantarkan arus listrik. Elektrolit adalah zat kimia yang menghasilkan partikel-partikel dengan muatan listrik. Berperan sebagai ion apabila berada dalam larutan.
Melansir Wikipedia, elektrolit merupakan suatu zat yang larut atau terurai menjadi bentuk ion. Kemudian larutan tersebut menjadi konduktor elektrik. Ion-ion merupakan atom-atom dengan muatan elektrik.
Sedangkan larutan elektrolit merupakan larutan yang dapat menghantarkan arus listrik. Dalam larutan elektrolit, molekulnya terurai menjadi partikel. Muatan listrik positif dan negatif menamainya sebagai ion.
Baca Juga: Larutan Elektrolit dan Non Elektrolit, Ciri-Ciri, Contoh, dan Perbedaannya
Ada ion positif yang dikenal dengan kation. Sedangkan ion negatif sebagai anion. Jumlah dari muatan ion positif dan ion negatif serupa. Sehingga muatan ion-ion dalam larutan netral. Ion-ion tersebut menghantarkan arus listrik.
Inilah Beberapa Jenis Larutan Elektrolit
Larutan elektrolit terbagi menjadi tiga macam. Untuk itu, ketahui beberapa jenis larutan berikut ini.
Larutan Elektrolit Kuat
Jenis larutan ini memiliki konsentrasi ion besar. Dengan kata lain, suatu zat kimia tertentu mengalami ionisasi secara sempurna 100% dalam air. Meskipun sudah terionisasi secara sempurna, namun zat tersebut tidak berarti larut semuanya dalam air.
Hal itu karena zat hanya sedikit larut dalam air, namun menghasilkan elektrolit kuat. Seperti halnya zat stronsium hidroksida Sr(OH)2.
Zat tersebut basa kuat, memiliki kelarutan yang rendah dalam air. Namun di dalam air, zat ini mengalami disosiasi secara sempurna. Sehingga akan menjadi ion Sr2+ dan ion OH–. Jenis larutan elektrolit memiliki beberapa karakteristik.
Mampu menghantarkan listrik dengan baik atau kuat. Zat dapat terionisasi atau terdisosiasi dengan sempurna. Mengenai derajat ionisasi = 1. Larutan ini akan menghasilkan nyala lampu yang lebih terang.
Selain itu, gelembung gasnya cukup banyak apabila melakukan uji coba untuk menghantarkan listrik. Jenis elektrolit kuat seperti pada larutan garam NaCl dan KCl. Larutan basa kuat seperti NaOH, Sr(OH)2, KOH, dan yang lainnya.
Larutan Elektrolit Lemah
Untuk jenis larutan ini, zat yang terionisasi dalam air hanya sedikit. Bahkan hanya sebagian saja. Hal itu karena setiap zat kimia memiliki sifat yang berbeda. Maka tidak semua zat tersebut dapat mengalami ionisasi secara sempurna saat dalam air.
Terdapat beberapa jenis zat yang hanya terdisosiasi sebagian. Bahkan hanya sedikit menghasilkan ion. Seperti halnya asam lemah dan basa lemah. Selain itu, sebagian besar molekul memiliki nitrogen.
Jenis larutan elektrolit memiliki beberapa karakteristik. Menghantarkan listrik dengan lemah. Bahkan dapat dikatakan kurang baik sebagai penghantar listrik. Zat hanya mengalami ionisasi atau terdisosiasi sebagian kecil saja. Derajat ionisasinya lebih dari 0, namun ternyata kurang dari 1.
Baca Juga: Senyawa Turunan Alkana Dengan Berbagai Gugus Fungsi yang Berbeda
Apabila melakukan uji coba untuk menghantarkan listrik, larutan elektrolit lemah akan menghasilkan nyala lampu yang tampak redup. Selain itu, menghasilkan hanya sedikit gelembung gas. Seperti halnya asam lemah CH3COOH, H3PO4, HCN, dan yang lainnya. Sedangkan untuk basa lemah seperti halnya NH4OH dan Al(OH)3.
Larutan Non Elektrolit
Jenis elektrolit ini adalah larutan zat yang sama sekali tidak terionisasi dalam air. Seperti pada elektrolit lemah, tidak semua zat dapat mengalami proses ionisasi dalam air. Bahkan terdapat beberapa zat yang sama sekali tidak mengalami ionisasi apabila melarutkannya dalam air.
Meskipun begitu, zat tersebut sebenarnya larut secara sempurna. Bahkan memiliki kelarutan yang terbilang tinggi dalam air. Saat zat tersebut tidak mengalami ionisasi, maka akan tetap saja sebagai non elektrolit.
Hal itu karena tidak memiliki ion-ion dalam larutan. Larutan tersebut pun tidak memiliki spesi yang dapat bergerak bebas dan bermuatan. Oleh karena itu, jenis larutan non elektrolit tidak dapat menghantarkan listrik.
Larutan non elektrolit memiliki karakteristik. Seperti tidak dapat menghantarkan listrik atau sifatnya isolator. Zat tidak dapat mengalami ionisasi dalam air, bahkan derajat ionisasi = 0.
Apabila melakukan uji coba untuk menghantarkan listrik, larutan non elektrolit tidak akan menghasilkan nyala pada lampu. Bahkan tidak adanya gelembung gas pada larutan ini. Seperti halnya pada larutan gula, etanol, lemak, dan yang lainnya.
Jenis larutan elektrolit umumnya dapat menghantarkan listrik. Larutan tersebut juga memiliki beberapa karakteristik khusus yang membedakan tiap jenisnya. (R10/HR Online)